Réanimation Néonatale
Recherche et Enseignement
Notre équipe est composée d’enseignants-chercheurs affiliés
au laboratoire de recherche INSERM U1059 SAINBIOSE de l’Université Jean Monnet . Ensemble, nous assurons nos missions d’enseignement et de recherche au niveau local, national, et international.
Maturation du système nerveux autonome
Chez le nouveau-né, l’évaluation du fonctionnement du système nerveux autonome (SNA) par l’étude en temps réel ou en différé de la variabilité intrinsèque de la fréquence cardiaque, en tant que témoin du fonctionnement de la régulation sympathovagale, permet d’appréhender les dysrégulations centrales de la commande cardiorespiratoire incriminées dans la physiopathologie des malaises graves, du syndrome de mort inattendue du nourrisson, et des bradycardies-apnées du prématuré. Nous savons maintenant, grâce à de nombreuses études menées au sein de notre laboratoire à partir de cohortes d’enfants prématurés comparés à des enfants à terme, que le niveau de maturation autonomique dépend étroitement de l’âge gestationnel et de l’âge postnatal. Nous avons également confirmé ce profil sur un modèle animal (agneau prématuré).
Pour mieux dessiner le profil de maturation autonomique dans la prime enfance, nous avons constitué la cohorte AuBE « Autonomic Baby Evaluation », forte de plus de 300 bébés suivis pour la première fois longitudinalement dès la naissance puis les premières années de vie, correspondant à une période de particulière vulnérabilité pour l’individu.
A partir de la cohorte AuBE, l’instabilité de la commande autonomique cardiaque a également été évaluée dans différentes conditions incluant l’exposition fœtale au tabagisme maternel, la dépression maternelle, ainsi que les différents stades de vigilance et de sommeil.
À 2 ans ½, nous avons confronté l’activité autonomique des enfants de la cohorte AUBE à leur développement neurocognitif, évalué par des tests neurodéveloppementaux afin de tester l’hypothèse selon laquelle le SNA pouvait être un marqueur sensible de dysfonctionnement neurologique non visible à l’imagerie.
Enfin, nous avons montré que le défaut de régulation autonomique observé en cas de prématurité se comblait au cours des deux premières années de vie.
Courbes lissées du développement du SDNN en fonction de l'âge et du sexe.
D’après Patural H, et al. Autonomic maturation from birth to 2 years: normative values. Heliyon (2019)
- Patural H, Pichot V, Roche F, Giraud A. Why, when and how to assess autonomic nervous system maturation in neonatal care units: A practical overview. Neurophysiologie Clinique (2023) 53: 102855.
- Patural H, Franco P, Pichot V, Giraud A. Heart rate variability analysis to evaluate autonomic nervous system maturation in neonates: an expert opinion. Frontiers in Pediatrics (2022) 10: 860145.
- Patural H, Pichot V, Flori S, Giraud A, Franco P, Pladys P, Beuchée A, Roche F, Barthelemy JC. Autonomic maturation from birth to 2 years: normative values. Heliyon (2019) 5: e01300.
- Franco P, Guyon A, Stagnara C, Flori S, Bat-Pitault F, Lin JS, Patural H. Early polysomnographic characteristics associated with neurocognitive development at 36 months of age. Sleep Med (2019) S1389-9457(19)30001-2
- Levieux K, Patural H, Harrewijn I, and OMIN Study Group. The French prospective multisite registry on sudden unexpected infant death (OMIN): rationale and study protocol. BMJ Open (2018) 17;8(4):e020883.
- Levieux K, Patural H, Harrewijn I, Briand Huchet E, Kugener B, Pidoux O, de Visme S, Adjaoud C, Gras Le Guen C, Hanf M; ANCReMIN. Sudden unexpected infant death: Time for integrative national registries. Arch Pediatr (2018) 25(2):75-76.
Cremillieux C, Makhlouf A, Pichot V, Trombert B, Patural H. Objective assessment of induced acute pain in neonatology with the Newborn Infant Parasympathetic Evaluation index. Eur J Pain (2018) 22(6):1071-1079.
- Plancoulaine, S ; Stagnara, C ; Flori, S ; Bat-Pitault, F ; Lin, JS ; Patural, H & al , Early features associated with the neurocognitive development at 36 months of age: the AuBE study. Sleep Med (2017) 30, 222-228.
- Bat-Pitault, F ; Sesso, G ; Deruelle, C ; Flori, S ; Porcher-Guinet, V ; Stagnara, C & al , Altered sleep architecture during the first months of life in infants born to depressed mothers. Sleep Med (2017) 30, 195-203.
- Gillioen, B ; Plancoulaine, S ; Montemitro, E ; Flori, S ; Lin, JS ; Guyon, A & al , Maturation of arousals during day and night in infants with non-smoking and smoking mothers. Early Hum Dev (2017) 115, 46-50.
Inflammation périnatale et développement de l’enfant
La période périnatale, c’est-à-dire entourant la naissance, est une période critique. Elle représente une étape majeure de la construction cérébrale et se caractérise par un pic de fabrication des principales cellules cérébrales, notamment des neurones, qui soutiendront le développement de l’enfant jusqu’à l’âge adulte. L’inflammation périnatale est définie comme la survenue d’une inflammation du placenta, appelée chorioamniotite, ou d’une infection bactérienne se déclarant dans les trois premiers jours de vie, appelée infection néonatale bactérienne précoce.
Chez l’enfant prématuré, l’inflammation périnatale constitue une lésion cérébrale précoce. À l’échelle endothéliale, elle dérégule de manière diffuse la barrière hémato-encéphalique. À l’échelle électroencéphalographique, celle-ci entraîne une altération de la maturation cérébrale. À l’échelle développementale, l’exposition à une inflammation périnatale est associée de manière indépendante à une diminution des capacités motrices globales et des capacités de socialisation.
Dans le cadre de l’accident vasculaire cérébral ischémique artériel néonatal, l’inflammation périnatale constitue un déterminant de lésion cérébrale précoce, en représentant à la fois un facteur de risque majeur et un mécanisme physiopathologique fondamental.
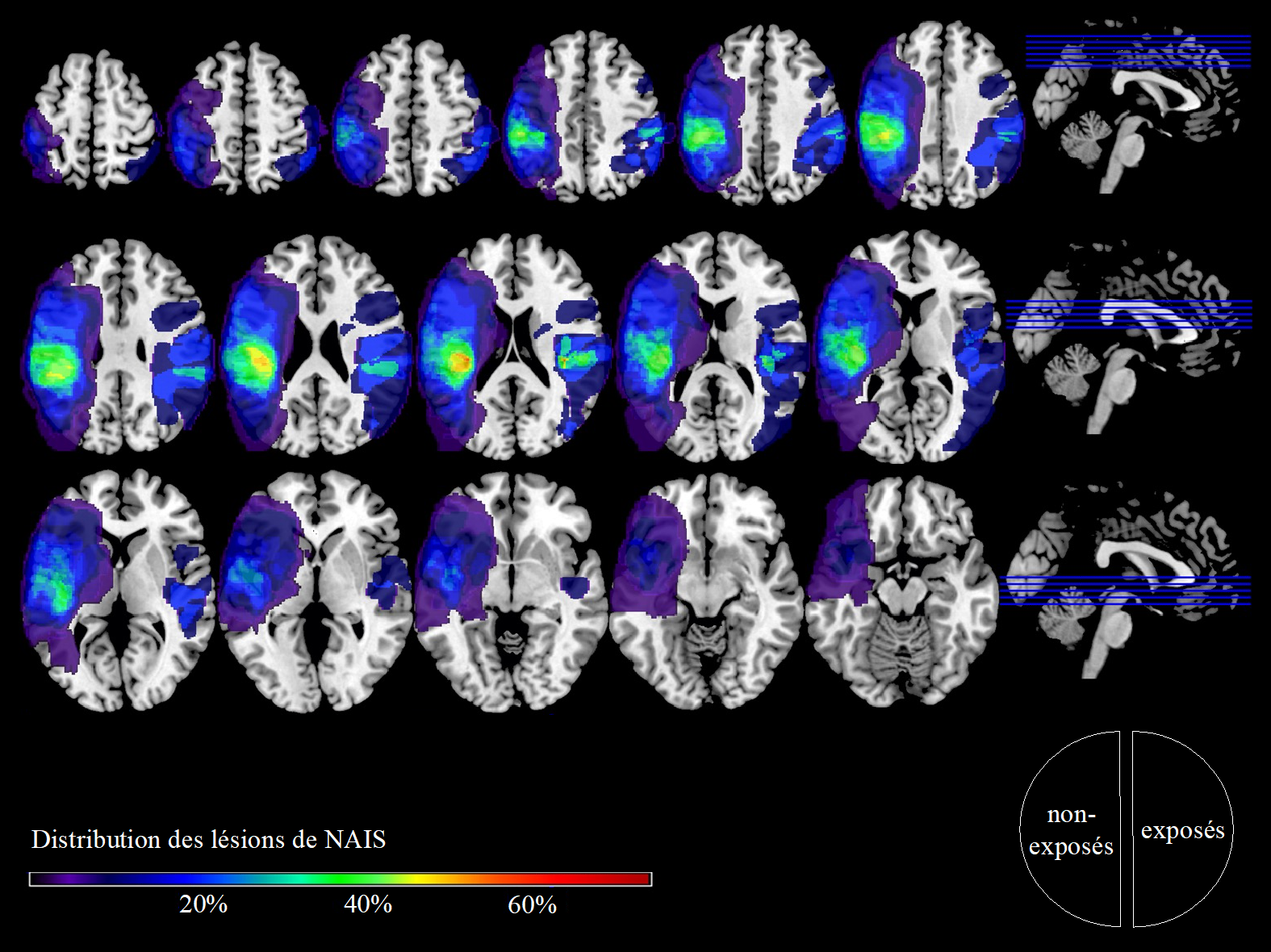
Cartographie des lésions d’accident vasculaire cérébral ischémique artériel néonatal à 7 ans des enfants exposés versus non exposés à une inflammation périnatale.
D’après Giraud A, et al. Perinatal inflammation exposure and developmental outcomes 7 years after neonatal arterial ischaemic stroke. Developmental Medicine & Child Neurology (2023)
- Giraud A, Dinomais M, Garel P, Chevin M, Thébault G, Renaud C, Presles E, Raia-Barjat T, Sébire G, Chabrier S. Perinatal inflammation exposure and developmental outcomes 7 years after neonatal arterial ischaemic stroke. Developmental Medicine & Child Neurology (2023) 65: 1073-1080.
- Giraud A, Stephens C, Boylan G, Walsh B. Conventional electroencephalography for accurate assessment of brain maturation in preterm infants following perinatal inflammation. Pediatric Research (2023) 93: 1118-1119.
- Giraud A, Stephens C, Boylan G, Walsh B. The impact of perinatal inflammation on the electroencephalogram in preterm infants: a systematic review. Pediatric Research (2022) 92: 32-39.
- Raia-Barjat T, Digonnet M, Giraud A, Ayash T, Vancolen S, Benharouga M, Chauleur C, Alfaidy N, Sébire G. Animal models of chorioamnionitis: Considerations for translational medicine. Biomedicines (2022) 10: 811.
- Giraud A, Chaux R, Allard MJ, Celle M, Teyssier G, Roche F, Chapelle C, Chabrier S, Sébire G, Patural H. Perinatal inflammation is associated with social and motor impairments in preterm children without severe neonatal brain injury. European Journal of Paediatric Neurology (2020) 28: 126-132.
- Giraud A, Allard MJ, Segura M, Roche F, Patural H, Sébire G. Ampicillin treatment increases placental interleukin-1 beta concentration and polymorphonuclear infiltration in group B Streptococcus-induced chorioamnionitis: a preclinical study. Neonatology (2020) 117: 369-373.
- Allard MJ, Giraud A, Segura M, Sébire G. Sex-specific maternofetal innate immune responses triggered by group B Streptococci. Scientific Reports (2019) 9: 8587
- Faure-Bardon V, Magny JF, Parodi M, Patural H. Sequelae of congenital cytomegalovirus (cCMV) following maternal primary infection are limited to those acquired in the first trimester of pregnancy. Clin Infect Dis (2019) 69(9):1526-1532
- Giraud A, Allard MJ, Roche F, Segura M, Patural H, Sébire G. Effet de l’antibiothérapie intrapartum sur l’inflammation placentaire dans un modèle murin de chorioamniotite à streptocoque de groupe b. Perfectionnement en Pédiatrie (2018) 1: 155-156.
- Giraud A, Guiraut C, Chevin M, Chabrier S, Sébire G. Role of perinatal inflammation in neonatal arterial ischemic stroke. Frontiers in Neurology (2017) 8: 612
Caractérisation du pleur des bébés et de sa perception
Le pleur du bébé est un signal vital codant des informations liées à son état motivationnel et physiologique, ainsi que des informations relatives à son identité. La fonction la plus communément admise du pleur est de solliciter l’attention d’adultes. Bien que la structure acoustique du pleur et les réponses des adultes à ce stimulus aient fait l’objet d’études depuis les années soixante-dix, l'information portée par les pleurs ainsi que les facteurs modulant la perception et la réaction aux pleurs des auditeurs adultes ne sont pas bien connus. Nous étudions ces questions avec l’équipe CNRS UMR9197 – ENES de l’Université Jean Monnet ,spécialisée dans les communications acoustiques.
En étudiant la signature vocale portée par les pleurs, nous avons démontré que chaque bébé pleure de manière distincte et les parents reconnaissent aisément leur propre bébé sur la base de ses seuls pleurs.
Par ailleurs, les pleurs des bébés filles et des bébés garçons ne peuvent être distingués sur la base de leur hauteur, car des individus des deux sexes peuvent pleurer dans l’aigu ou dans le grave. Pourtant les adultes pensent pouvoir évaluer la féminité ou la masculinité des bébés rien qu’en écoutant leurs pleurs. De plus, les hommes adultes considèrent que des pleurs présentés comme « garçons » expriment plus d’inconfort que les mêmes pleurs présentés comme « filles ».
Beaucoup reste à apprendre sur la manière dont les adultes perçoivent et décodent les informations portées par les pleurs de bébés. Nous cherchons à caractériser avec l'équipe ENES les paramètres acoustiques permettant de coder l’intensité de douleur dans les pleurs.
D’après Aurélie Plat. Ontogénèse de la reconnaissance vocale du pleur du nouveau-né par sa mère. Thèse d’Exercice (2014)
- Corvin S, Fauchon C, Patural H, Peyron R, Reby D, Theunissen F, Mathevon N. Pain cues override identity cues in baby cries. iScience (2024) 27(7):110375.
- Lockhart-Bouron M, Anikin A, Pisanski K, Corvin S, Cornec C, Papet L, Levréro F, Fauchon C, Patural H, Reby D, Mathevon N. Infant cries convey both stable and dynamic information about age and identity. Commun Psychol (2023) 1, 26.
- Bouchet H, Plat A, Levrero F, Reby D, Patural H, Mathevon N. Baby cry recognition is independent of motherhood but improved by experience and exposure. Proceedings Royal Society B (2020) 287, 20192499.
- Koutseff A, Reby D, Martin O, Levrero F, Patural H, Mathevon N. The acoustic space of pain: cries as indicators of distress recovering dynamics in pre-verbal infants. Bioacoustics (2017) 27(4), 313–325.
Automatisation de l’évaluation des mouvements généraux
L'évaluation des mouvements généraux analyse la complexité, la variabilité et la fluidité des mouvements que les enfants prématurés produisent spontanément, avant l’apparition d’une motricité volontaire. Cette évaluation fonctionnelle cérébrale précoce, réalisée au sein du service de Néonatalogie, permet d'identifier les enfants présentant une trajectoire développementale anormale, et d’initier une intervention individualisée précoce dès la sortie d’hospitalisation. Cependant, l'évaluation des mouvements généraux reste subjective et chronophage, limitant son utilisation en pratique clinique.
C’est pourquoi nous développons, à l’aide d’outils de computer vision et d'intelligence artificielle, une analyse automatisée de ces mouvements généraux dans le cadre de l’étude AGMA (Élaboration d’un outil pronostique développemental de l’enfant prématuré basé sur l’analyse automatisée de la motricité spontanée ; Numéro IDRCB 2020-A03335-34). Cette étude est réalisée en collaboration avec le laboratoire CNRS U5516 – Hubert Curien, de l’Université Jean Monnet , spécialisée dans le traitement d’image
Afin de promouvoir l’évaluation des mouvements généraux dans les unités de Néonatalogie, nous avons développé le programme informatique AGMA-PESS (https://doi.org/10.3389/fped.2024.1465632). Librement téléchargeable et utilisable, ce logiciel permet de fournir une estimation de pose des enfants et de sélectionner automatiquement les séquences d’intérêt à partir de vidéos destinées à l’évaluation des mouvements généraux.

Estimation de la pose dans les trois plans de l’espace par méthode d’intelligence artificielle
D’après Soualmi A, et al. A 3D pose estimation framework for preterm infants hospitalized in the Neonatal Unit. Multimedia Tools and Applications (2023).
- Soualmi A, Alata O, Ducottet C, Petitjean-Robert A, Plat A, Patural H, Giraud A. AGMA-PESS: a deep learning-based infant pose estimator and sequence selector software for General Movement assessment. Frontiers in Pediatrics (2024) 12: 1465632.
- Soualmi A, Ducottet C, Patural H, Giraud A, Alata O. A 3D pose estimation framework for preterm infants hospitalised in the Neonatal Unit. Multimedia Tools & Applications (2023) 83: 24383-24400.
- Soualmi A, Alata O, Ducottet C, Patural H, Giraud A. Mean 3D Dispersion for Automatic General Movement Assessment of Preterm Infants. Annual International Conference of the IEEE Engineering in Medicine and Biology Society (2023) 1-5.